Tlenki i utlenianie
Tlenki to związki chemiczne, które powstają, gdy tlen reaguje z innymi pierwiastkami. Taka reakcja nazywa się utlenianiem. Jeśli przebiega gwałtownie i towarzyszy jej wydzielanie światła oraz ciepła, mówimy o spalaniu.
- Utlenianie – reakcja pierwiastka z tlenem, w wyniku której powstaje tlenek.
- Spalanie – szybkie utlenianie połączone z wydzielaniem energii.
Tworzenie wzoru tlenków
Tlenki to dwuskładnikowe związki tlenu z innymi pierwiastkami.
Wzór ogólny tlenków: XaOb
| X - atom dowolnego pierwiastka | a - ilość atomów pierwiastka X |
| O - atom tlenu | b - ilość atomów tlenu |
Jak ustala się wzór tlenku metodą krzyżową?
Przenosi się wartościowość jednego pierwiastka za symbol drugiego pierwiastka. Powstałe indeksy dzieli się przez największy wspólny dzielnik.
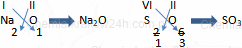
Większość wzorów sumarycznych można w taki sposób wyprowadzić, jednak są wyjątki np. P4O10. Sumaryczny wzór tego tlenku wynika z jego struktury.
Jak tworzy się nazwy tlenków
Nazwy tlenków tworzy się według prostych zasad:
- Zaczyna się od słowa „tlenek”.
- Dodaje się nazwę pierwiastka.
- Jeśli pierwiastek ma więcej niż jedną wartościowość, podaje się ją w nawiasie rzymskim.
tlenek + nazwa pierwiastka + (wartościowość pierwiastka)
Przykłady nazw tlenków
CO – tlenek węgla(II)
CO2 – tlenek węgla(IV) - nazwa zwyczajowa: dwutlenek węgla
FeO – tlenek żelaza(II)
Fe2O3 – tlenek żelaza(III)
SO2 – tlenek siarki(IV)
SO3 – tlenek siarki(VI)
P4O10 – tlenek fosforu(V)
N₂O – tlenek azotu(I)
N2O5 – tlenek azotu(V)
SiO2– tlenek krzemu(IV)
Jak otrzymuje się tlenki
Tlenki otrzymuje się, gdy tlen reaguje z innymi pierwiastkami. Jest to reakcja syntezy. Sposób przebiegu zależy od rodzaju pierwiastka i warunków, np. temperatury.
1. Jak reagują metale z tlenem?
Wapń - łatwo reaguje z tlenem tworząc tlenek wapnia
2Ca + O2 → 2CaO
wapń + tlen → tlenek wapnia
Magnez – w kontakcie z tlenem spala się, tworząc tlenek magnezu.
2Mg+O2 → 2MgO
magnez + tlen → tlenek magnezu
Żelazo – w warunkach wysokiej temperatury żelazo reaguje z tlenem, tworząc tlenek żelaza(III)
3Fe + 2O2→Fe2O3
żelazo + tlen → tlenek żelaza(III)
Sód – łatwo reaguje z tlenem, tworząc tlenek sodu.
4Na+O2→2Na2O
sód + tlen → tlenek sodu
2. Jak reagują niemetale z tlenem?
Węgiel – spalanie węgla w tlenie prowadzi do powstania tlenku węgla(IV) (CO₂), przy niepełnym spalaniu może też powstać tlenek węgla(II) (CO).
C + O2 → CO2
2C + O2 → 2CO
Siarka – w reakcji z tlenem tworzy tlenek siarki (IV).
S + O2 → SO2
Fosfor – w kontakcie z tlenem fosfor pali się, tworząc tlenek fosforu(V) (P₄O₁₀).
4P + 5O2 → P4O10
Jakie tlenki spotykamy na co dzień?
Wiele tlenków występuje w przyrodzie i produktach codziennego użytku. Oto kilka przykładów:
Tlenek węgla(IV) CO2
- Nazwa zwyczajowa: dwutlenek węgla
- Jest produktem oddychania.
- Potrzebny roslinom do fotosyntezy.
- Używany w napojach gazowanych i gaśnicach śniegowych.
Tlenek wapnia CaO
- Nazwa zwyczajowa: wapno palone
- Do produkcji cementu i zapraw murarskich.
- W oczyszczaniu wody i gleby.
Tlenek żelaza(III) Fe2O3
- Powstaje na powierzchni metali jako wynik korozji.
- Może być składnikiem farb antykorozyjnych.
Tlenek siarki(IV) SO2
- Nazwa zwyczajowa: dwutlenek siarki
- W przemyśle spożywczym jako konserwant (E220).
- Powstaje podczas spalania węgla i może powodować zanieczyszczenie powietrza (kwaśne deszcze).
Tlenek wodoru H2O
- Nazwa zwyczajowa: woda
- Niezbędna do życia wszystkich organizmów.
- Stosowana do picia, gotowania, mycia i nawadniania roślin.
- Rozpuszcza wiele substancji, np. sól czy cukier.
Tlenek krzemu(IV) SiO2
- Nazwa zwyczajowa: krzemionka, piasek
- Główny składnik plaż, pustyń i budowlanych zapraw.
- Do produkcji szkła, ceramiki i betonu.
- W niektórych kosmetykach i pastach do zębów.
Tlenek glinu Al2O3
- Nazwa systematyczna: tlenek glinu
- Do produkcji papieru ściernego i narzędzi szlifierskich.
- Naturalna forma tlenku glinu to szafir i rubin – cenne kamienie szlachetne.
Tlenki są wszędzie wokół nas – w powietrzu, glebie, wodzie i produktach codziennego użytku. Niektóre są przydatne, inne mogą być szkodliwe. Warto wiedzieć, jak wpływają na nasze życie!
Jakie właściwości i inne zastosowania mają tlenki? (rozszerzenie)
Tlenek wapnia CaO
Tlenek wapnia, zwany również wapnem palonym, to biały, krystaliczny proszek o szerokim zastosowaniu w przemyśle i budownictwie. Powstaje w wyniku termicznego rozkładu wapienia (CaCO₃) w procesie zwanym prażeniem wapienia.
Właściwości tlenku wapnia
1. Biały, krystaliczny proszek.
2. Stały stan skupienia.
3. Temperatura topnienia około 2 572 °C, co oznacza, że jest bardzo ogniotrwały.
4. Słabo rozpuszczalny, ale reaguje z wodą, tworząc wodorotlenek wapnia (wapno gaszone) w procesie egzotermicznym.
Zastosowanie tlenku wapnia
1. Budownictwo. Stosowany do produkcji zapraw murarskich i tynków. W reakcji z wodą (gaszenie wapna) powstaje wapno gaszone (Ca(OH)₂), które po zmieszaniu z piaskiem daje zaprawę murarską..
2. Przemysł chemiczny. Wykorzystywany do produkcji wapna gaszonego (Ca(OH)₂), stosowany w procesach produkcji szkła, gdzie pomaga usuwać zanieczyszczenia.
3. Oczyszczanie gazów. Stosowany w elektrowniach i zakładach przemysłowych do neutralizowania kwaśnych gazów (takich jak dwutlenek siarki SO₂), które mogą prowadzić do zanieczyszczeń powietrza i kwaśnych deszczy.
4. Rolnictwo. Używany do odkwaszania gleby, co poprawia warunki wzrostu roślin, stosowany do dezynfekcji gleby i oczyszczania wody w stawach.
Tlenek glinu Al2O3
Tlenek glinu (Al₂O₃), znany także jako korund lub alumina, to biały, krystaliczny związek chemiczny o dużej twardości i odporności chemicznej. Jest szeroko wykorzystywany w przemyśle dzięki swoim wyjątkowym właściwościom fizycznym i chemicznym.
Właściwości tlenku glinu
1. Biały proszek lub krystaliczna substancja o dużej twardości.
2. Stan skupienia stały.
3. Temperatura topnienia około 2 072 °C – bardzo wysoka, co sprawia, że jest odporny na działanie wysokich temperatur.
4. Twardość - jest jednym z najtwardszych materiałów naturalnych (9 w skali Mohsa), ustępującym tylko diamentowi.
Zastosowanie tlenku glinu
1. Przemysł metalurgiczny. Jest głównym surowcem do produkcji glinu (aluminium) w procesie elektrolizy w przemyśle metalurgicznym. Wykorzystywany do produkcji stopów aluminium, które są cenione za lekkość i wytrzymałość.
2. Przemysł materiałów ściernych. Ze względu na dużą twardość, tlenek glinu jest stosowany do produkcji materiałów ściernych, takich jak papiery ścierne i tarcze do szlifowania. Korund, naturalna odmiana Al₂O₃, jest wykorzystywany w produkcji kamieni szlifierskich.
3. Przemysł ceramiki i szkła. Stosowany do produkcji wytrzymałej ceramiki oraz szkła laboratoryjnego, które są odporne na działanie wysokich temperatur i chemikaliów. Używany również jako składnik materiałów ogniotrwałych.
4. Jubilerstwo. Czysty, krystaliczny tlenek glinu tworzy kamienie szlachetne, takie jak rubin i szafir, które są cenione za swoją twardość i atrakcyjne barwy. Dodatek pierwiastków chromu (rubin) lub żelaza i tytanu (szafir) nadaje Al₂O₃ charakterystyczne kolory.
5. Katalizatory: Tlenek glinu jest stosowany jako nośnik katalizatora w wielu reakcjach chemicznych, np. w przemyśle petrochemicznym, gdzie wspomaga procesy krakingu i oczyszczania.
Tlenek żelaza(III) Fe2O3
Tlenek żelaza(III), znany również jako hematyt lub rdza, to jeden z najczęściej spotykanych tlenków żelaza. Jest szeroko stosowany w przemyśle, a także naturalnie występuje w minerałach i rudach żelaza.
Właściwości tlenku żelaza(III)
1. Czerwono-brązowy proszek lub kryształy.
2. Stały stan skupienia.
3. Temperatura topnienia około 1 565 °C.
4. Jest stosunkowo twardy i odporny na działanie warunków atmosferycznych.
Zastosowanie tlenku żelaza(III)
1. Przemysł metalurgiczny. Jest kluczowym składnikiem do produkcji żelaza i stali. Fe₂O₃ jest głównym składnikiem rudy żelaza, którą redukuje się do czystego żelaza w wielkich piecach.
2. Produkcja pigmentów. Tlenek żelaza(III) jest stosowany jako pigment czerwono-brązowy w farbach, lakierach i tuszach. Zapewnia trwały kolor odporny na działanie światła i temperatury.
3. Ceramika i szkło. Używany w produkcji wyrobów ceramicznych i szkła jako barwnik, nadając im czerwono-brązowy kolor.
4. Magnetyczne nośniki danych. Fe₂O₃ jest stosowany do produkcji magnetycznych taśm i dysków twardych, gdzie wykorzystywana jest jego zdolność do namagnesowania i przechowywania informacji.
5. Przemysł kosmetyczny. Znajduje zastosowanie jako barwnik w produktach kosmetycznych, takich jak pudry, cienie do powiek i szminki, ze względu na bezpieczeństwo stosowania na skórze i trwałość koloru.
Tlenek siarki(IV)
Właściwości
1. Bezbarwny gaz (w warunkach standardowych) o intensywnym, drażniącym zapachu.
2. Łatwo rozpuszczalny w wodzie, tworzy kwas siarkowy(IV)
2. Nie jest palny.
Zastosowanie tlenku siarki(IV)
-
Przemysł chemiczny. Używany do produkcji kwasu siarkowego(VI) (H₂SO₄), który jest jednym z najważniejszych chemikaliów stosowanych w różnych procesach przemysłowych.
-
Środek dezynfekujący i konserwujący. Ze względu na swoje właściwości antybakteryjne i przeciwgrzybicze, SO₂ stosowany jest do konserwacji żywności, zwłaszcza suszonych owoców oraz wina, gdzie zapobiega psuciu i zmianom barwy.
-
Przemysł papierniczy. Używany w procesie bielenia masy celulozowej, który usuwa ligninę z drewna i pomaga uzyskać jasny papier.
-
Środowisko i ochrona przeciwpożarowa: Dwutlenek siarki jest używany jako gaz ochronny i do tworzenia specjalnych warunków atmosferycznych w różnych gałęziach przemysłu, choć ze względu na toksyczność jego stosowanie jest ograniczone.
Wpływ tlenku siarki(IV) na środowisko
- Kwaśne deszcze: SO₂, reagując z wodą, tlenem i innymi substancjami w atmosferze, tworzy kwasy siarkow, które przyczyniają się do powstawania kwaśnych deszczy. Kwaśne deszcze niszczą rośliny, zakwaszają gleby i zanieczyszczają wody, co wpływa negatywnie na ekosystemy.
- Zanieczyszczenie powietrza: Jest jednym z głównych składników smogu siarkowego i może powodować problemy zdrowotne, szczególnie u osób z chorobami układu oddechowego.
Tlenek siarki(VI) SO3
Właściwości tlenku siarki(VI)
1. W temperaturze pokojowej występuje jako bezbarwna ciecz. W temperaturze około 16,9 °C topi się, a w około 45 °C sublimuje do postaci gazowej.
2. Jest silnie higroskopijny – w kontakcie z wodą gwałtownie reaguje, tworząc kwas siarkowy(VI) (H₂SO₄).
3. Ze względu na dużą reaktywność, w kontakcie z wilgocią może powodować korozję i uszkodzenia materiałów.
Zastosowanie tlenku siarki(VI)
1. Produkcja kwasu siarkowego:SO₃ jest kluczowym surowcem w przemyśle chemicznym, wykorzystywanym do produkcji kwasu siarkowego(VI) (H₂SO₄) – jednego z najważniejszych kwasów przemysłowych stosowanego w produkcji nawozów, detergentów, barwników i materiałów wybuchowych.
2. Przemysł petrochemiczny. Tlenek siarki(VI) jest używany do otrzymywania środków powierzchniowo czynnych, takich jak detergenty i emulgatory.
Wpływ na środowisko i zdrowie
Działanie drażniące: SO₃ może powodować podrażnienia dróg oddechowych, skóry i oczu. W kontakcie z błonami śluzowymi przekształca się w kwas siarkowy, co może powodować uszkodzenia tkanek.
Kwaśne deszcze: Emisja SO₃ do atmosfery przyczynia się do powstawania kwaśnych deszczy, co wpływa destrukcyjnie na roślinność, gleby oraz wodne ekosystemy.
Tlenek krzemu(IV) SiO2
Tlenek krzemu(IV) , znany także jako krzemionka, jest jednym z najpowszechniejszych związków chemicznych w skorupie ziemskiej. Występuje naturalnie w różnych formach, takich jak kwarc, piasek, ametyst, czy kryształ górski.
Właściwości tlenku krzemu(IV)
1. Bezbarwne lub białe ciało stałe, może mieć różną przezroczystość (od całkowicie przezroczystego do mętnego).
2. W normalnych warunkach SiO₂ występuje jako twarde ciało stałe, które tworzy sieć krystaliczną, co nadaje mu dużą wytrzymałość.
3. Topi się w bardzo wysokiej temperaturze – około 1713 °C.
4. Jest bardzo twardy (7 w skali Mohsa), co sprawia, że jest odporny na zarysowania i ścieranie.
5. Jest nierozpuszczalny w wodzie i większości kwasów.
6. Jest chemicznie stabilny i mało reaktywny w warunkach standardowych, co sprawia, że jest odporny na działanie większości kwasów.
Zastosowanie tlenku krzemu(IV)
1. Budownictwo. Jest głównym składnikiem piasku i żwiru, stosowanym do produkcji betonu, cegieł, zapraw i innych materiałów budowlanych.
2. Przemysł ceramiczny i szklarski: Tlenek krzemu(IV) jest wykorzystywany do produkcji ceramiki, porcelany oraz szkła laboratoryjnego i optycznego.Krzemionka jest kluczowym surowcem do produkcji szkła, w którym SiO₂ stanowi podstawowy składnik.
3. Elektronika. Wykorzystuje się go w przemyśle elektronicznym, m.in. jako izolator w tranzystorach oraz w produkcji półprzewodników i układów scalonych.
4. Medycyna. Krzemionka stosowana w formie żeli do produkcji materiałów opatrunkowych oraz jako składnik implantów i materiałów dentystycznych.
